
化学基礎 物質の変化07 モル質量の求め方 13分 Youtube
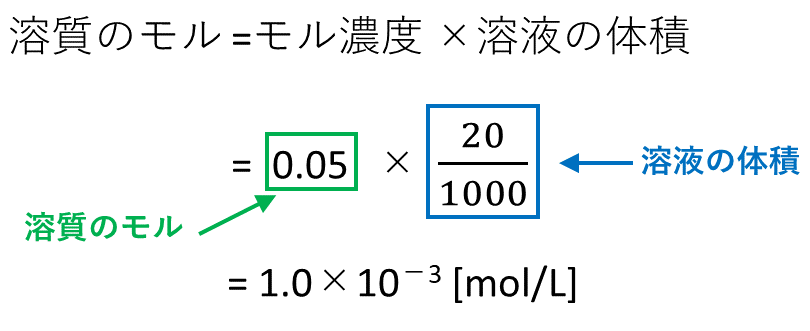
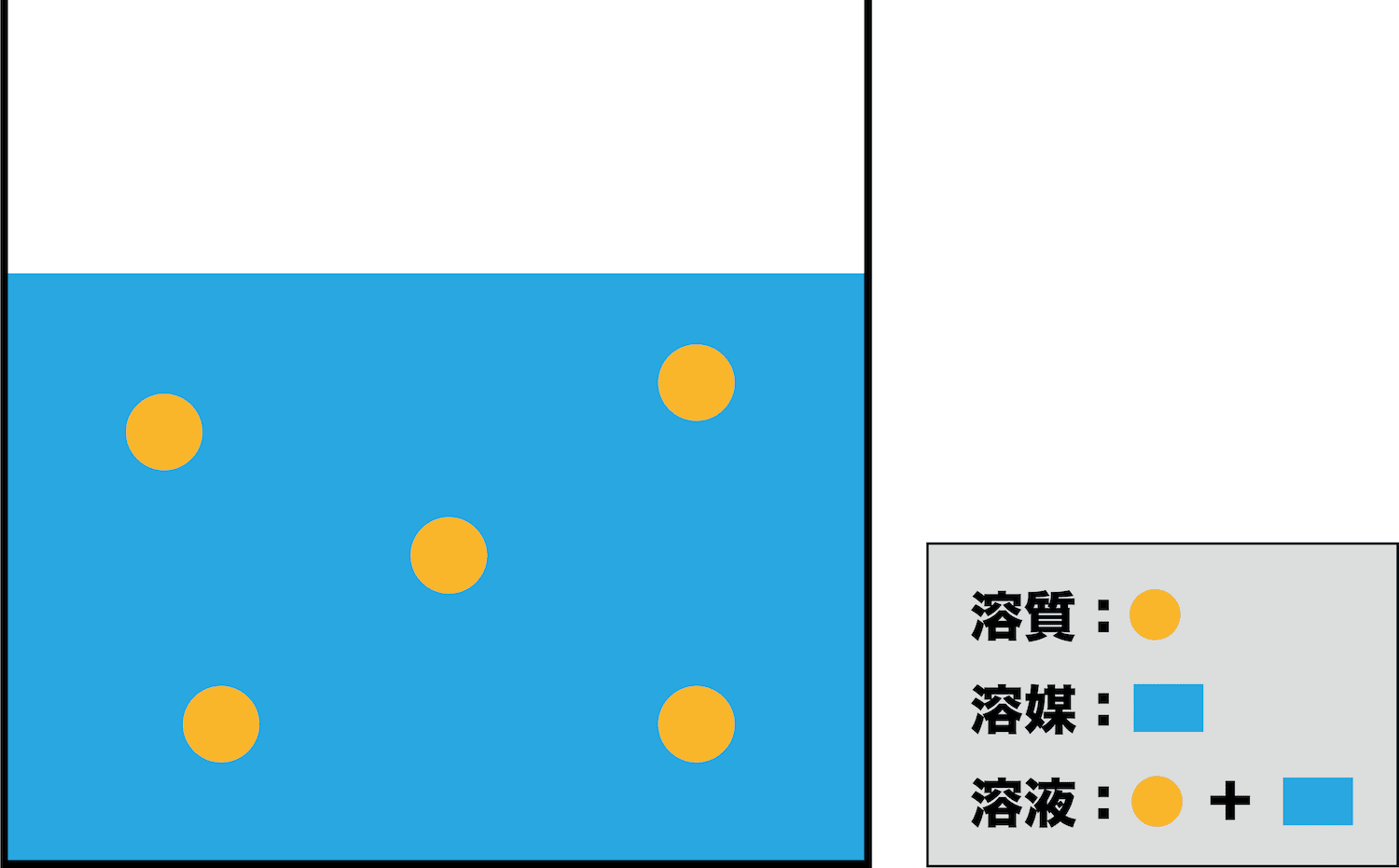
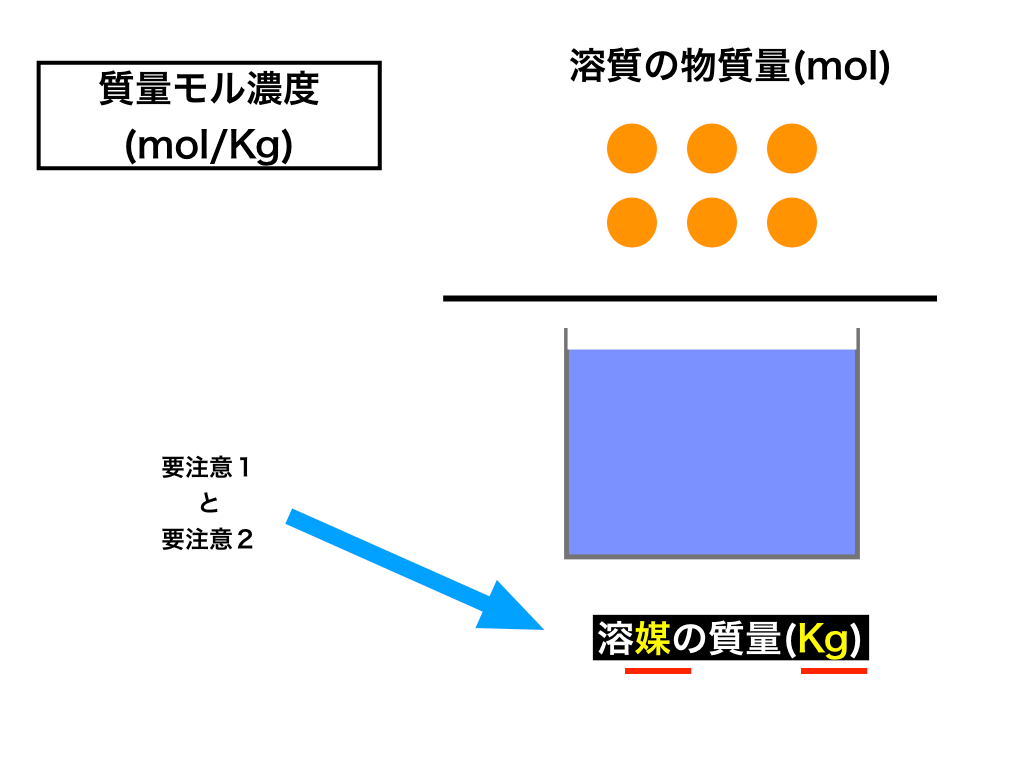
解答:1質量モル濃度2mol/kg 質 量 モ ル 濃 度 溶 質 溶 媒 質 量 モ ル 濃 度 ( m o l / k g) = 溶 質 ( m o l) 溶 媒 ( k g) 問4 に当てはまる用語を答えよ。 溶液に含まれる溶質の割合を表した濃度を1といい、単位は2である。 問4解答/解説 ME=10ε M分子量 E比吸光度 εモル吸光係数 (イプシロン)
モル 公式 覚え方
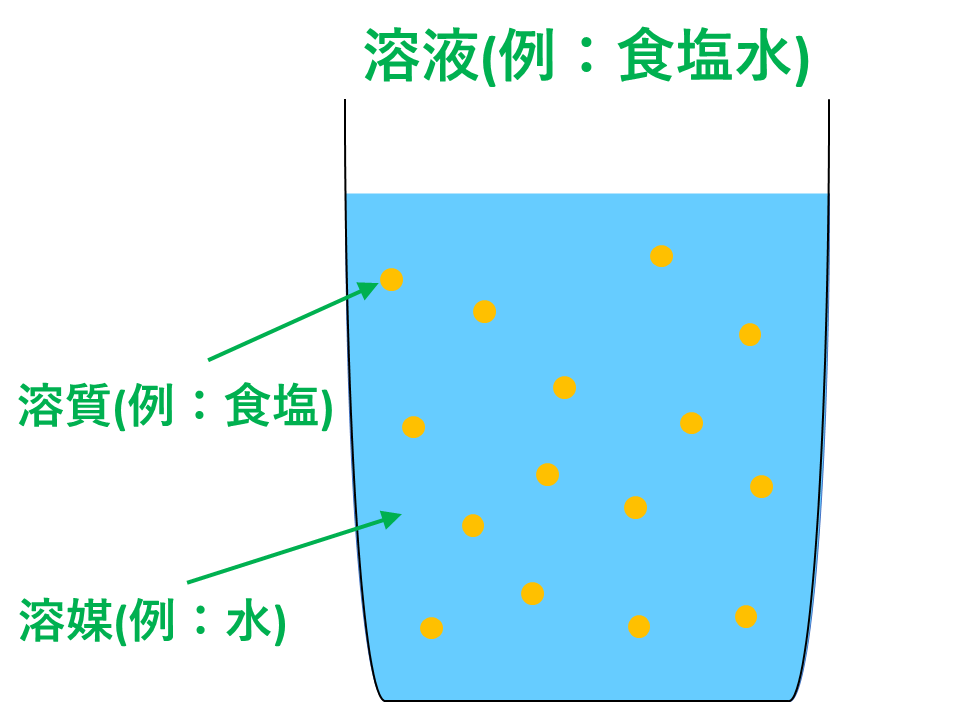
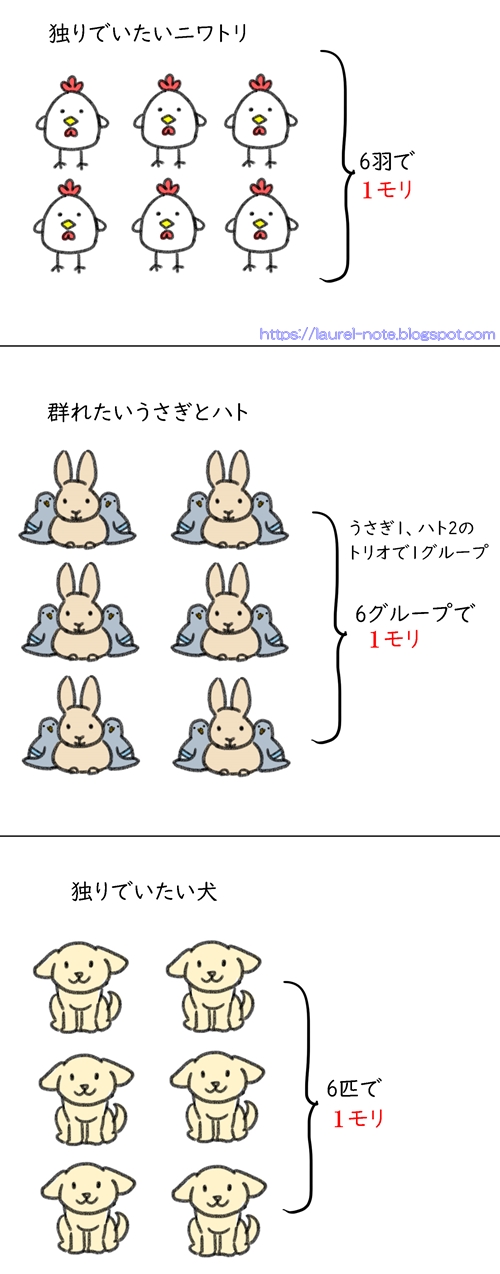
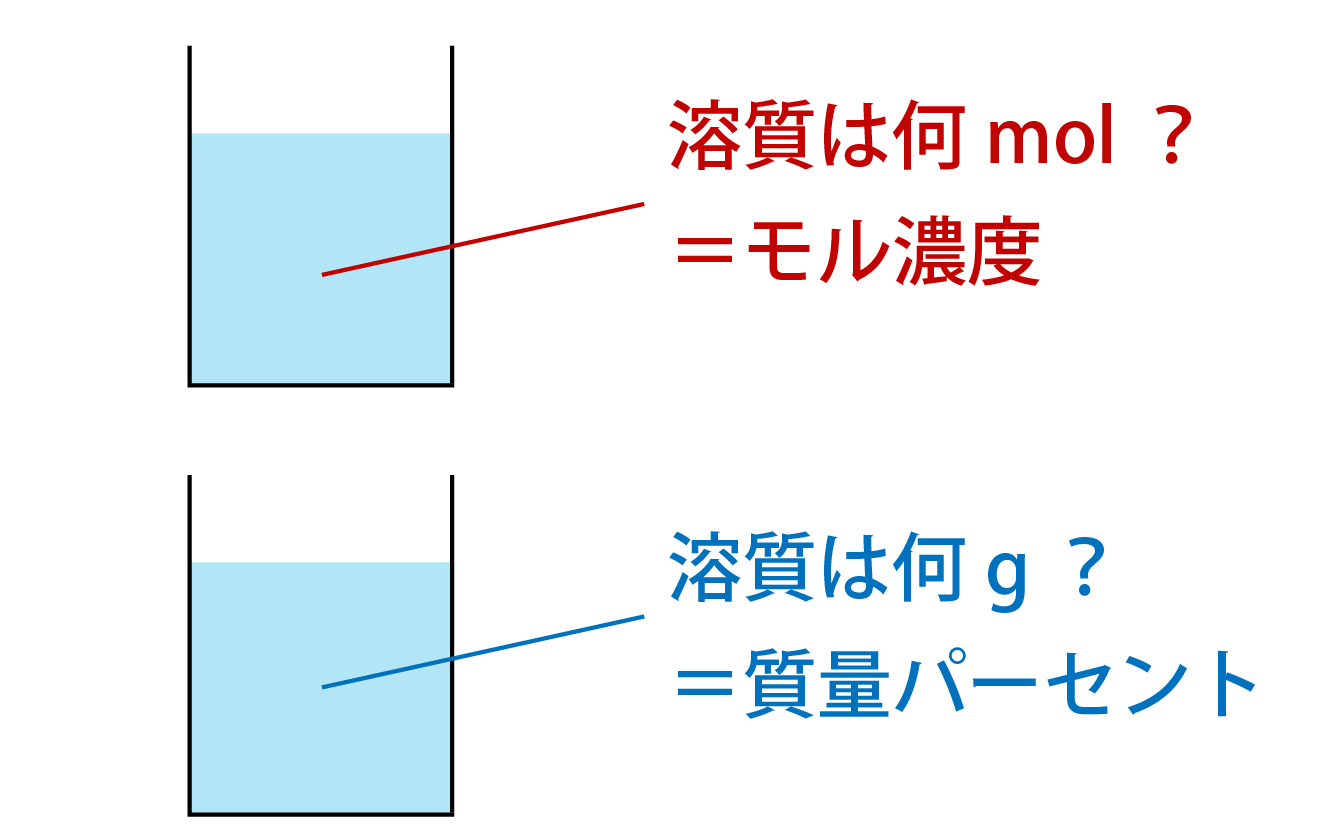
モル 公式 覚え方- サマリー ・モルの考え方は,ダースやカートンと似ています. ・分子生物学用エタノールは70 v/v%,消毒用エタノールは 769~814 v/v%です. ・濃度だけでなく,物質の絶対量も重要です. 目次 濃度の単位 モル濃度(Mまたはmol/L) パーセント濃度 重量 質量パーセント濃度・モル濃度・質量モル濃度 の3つの濃度を習います。 多くの高校生が濃度計算でつまづくのは、 これらの定義をきちんと覚えられていないからです。 まずは濃度の定義を覚えていくのが第一段階ですね。
放課後化学講義室 公式は問題に書いてある
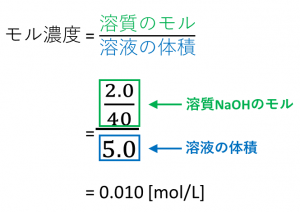
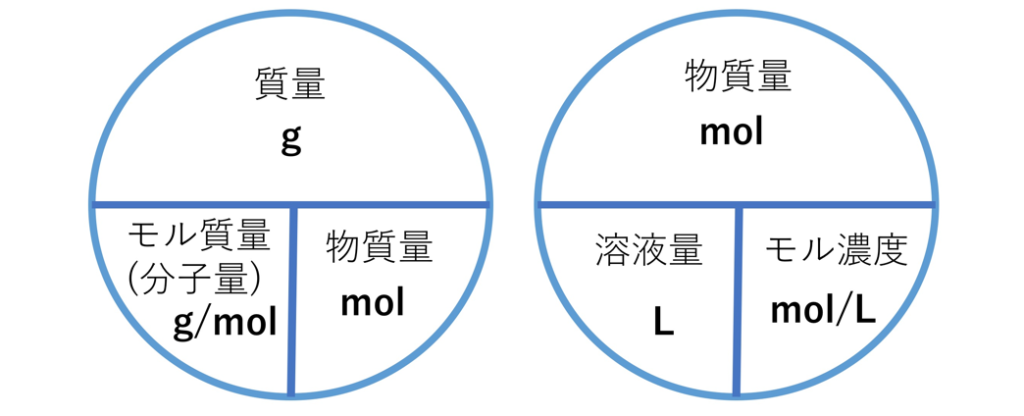
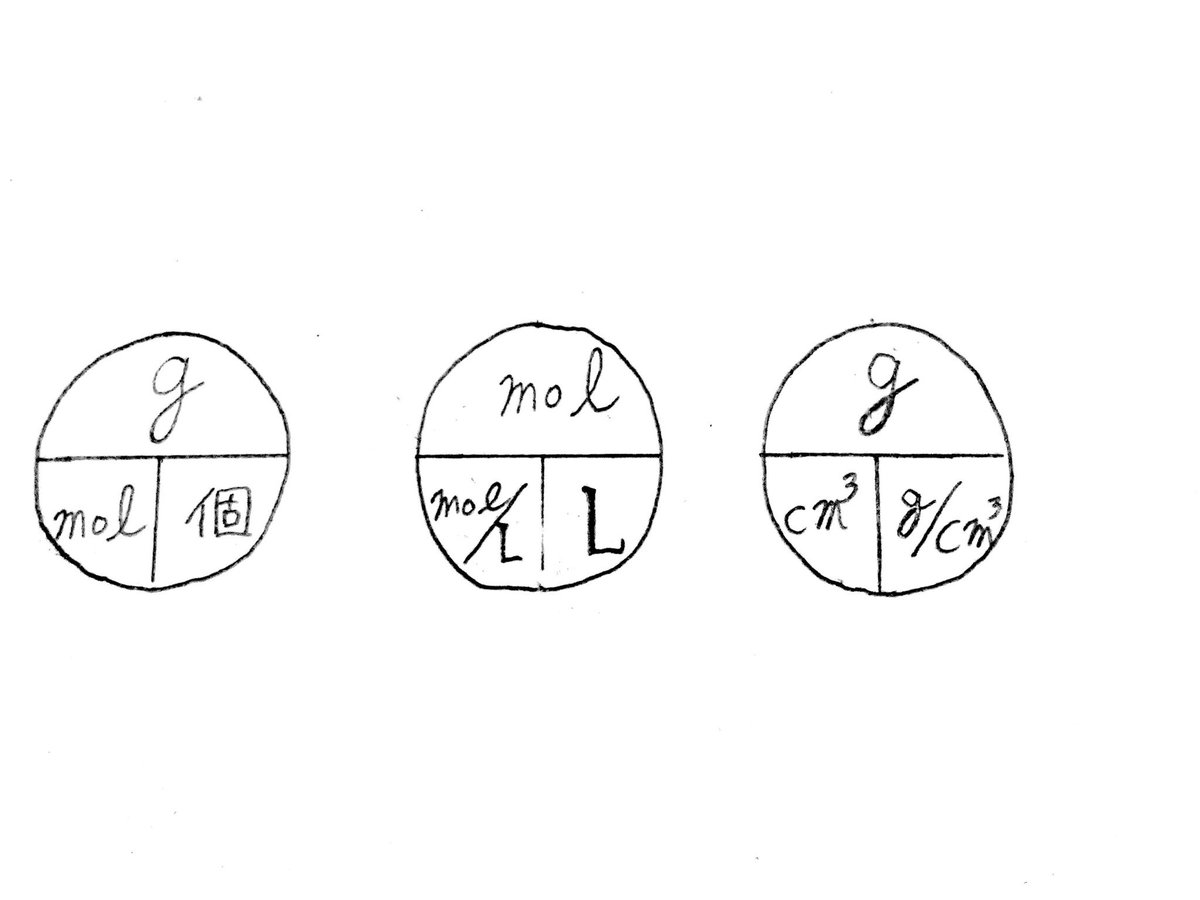
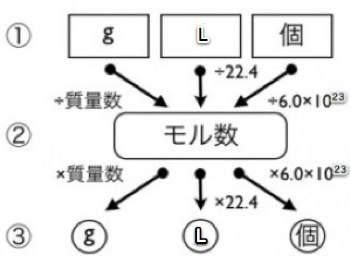
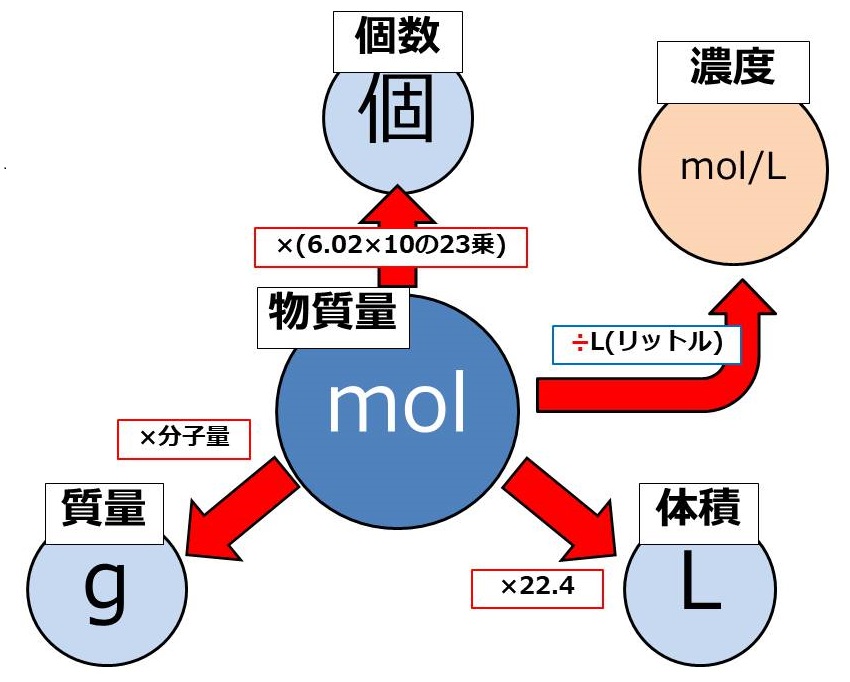
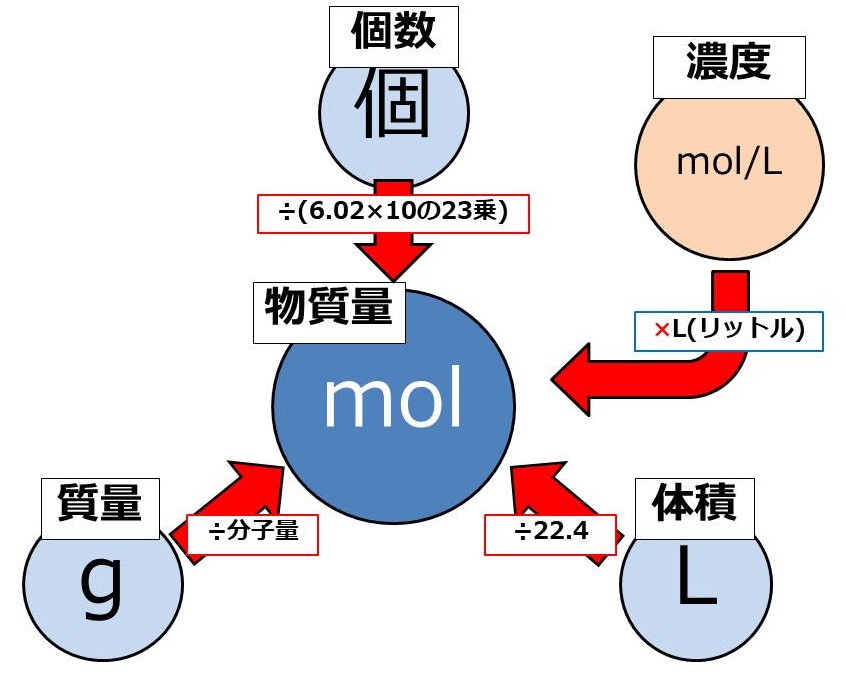
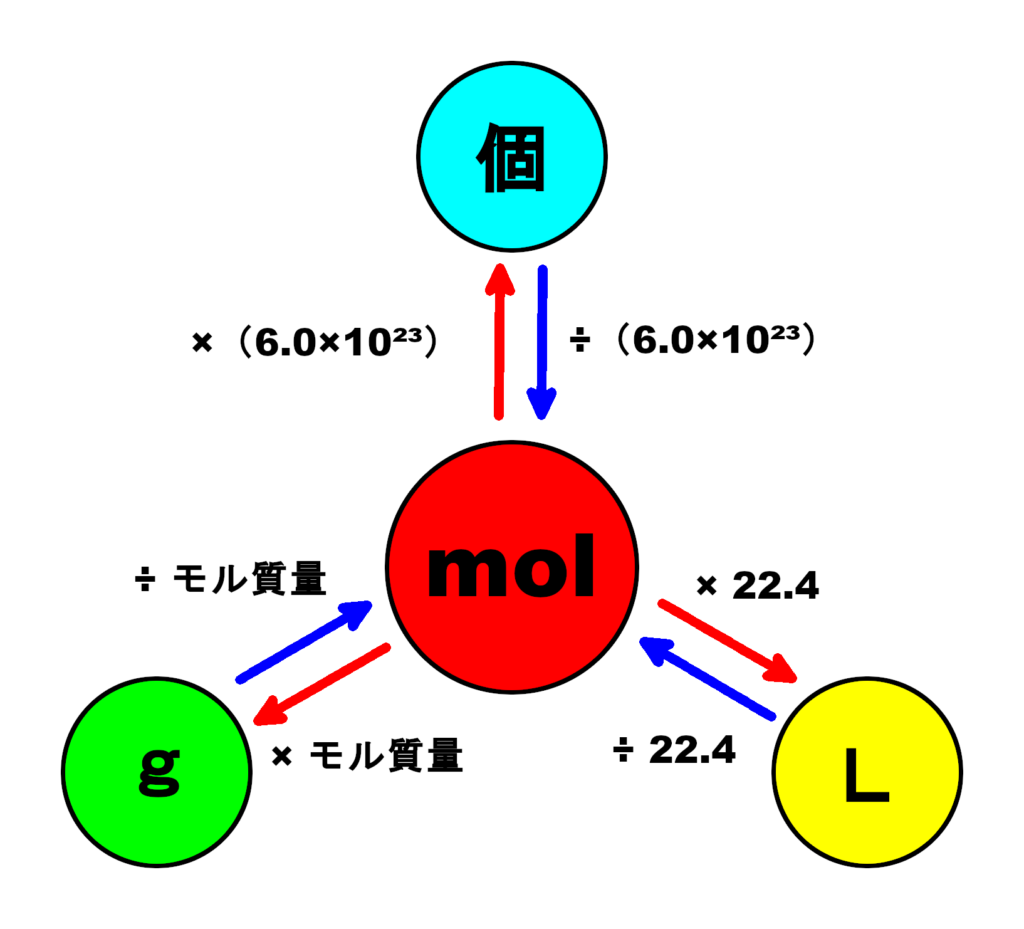
質量(g;グラム)、分子の個数(個)、気体の体積(L;リットル)の それぞれの間にあるのが、mol(モル)という単位 です。 必ずこのmolを通らないと計算が出来ないようになっています。 さて、molをどのように求めるのかというと、次の4パターンが基本です。 g (グラム) ÷ 分子量 = mol 気体のL (リットル) ÷ 224 = mol 分子の個数 ÷ アボガドロ定数 = mol 溶液の濃度 (mol/L) × 溶液のL (物質1molあたりの質量は、原子量・分子量・式量に単位〔g〕をつけたもの まずは、 (1)です。 問題文より、アルミニウム Al の原子量は27です。 ということは、アルミニウム1molあたりの質量は、 27g です。 このことから、比例式を立ててみましょう。 1mol27g= 3mol x g x=81 よって、答えは、 81g です。 次は、 (2)です。 (モル濃度(mol/L))=(mol)÷(L) F(kg・m/s 2)=(kg)×(m/s 2) ((kg・m/s 2)=(N)) と覚えましょう! ゴロや見た目は悪くても、覚えてしまえば実際にテストで生きる公式になります! 注意はひとつだけ、(kg・m/s 2)は(N)とすることが決められています。ニュートンさんの頭文字ですね。
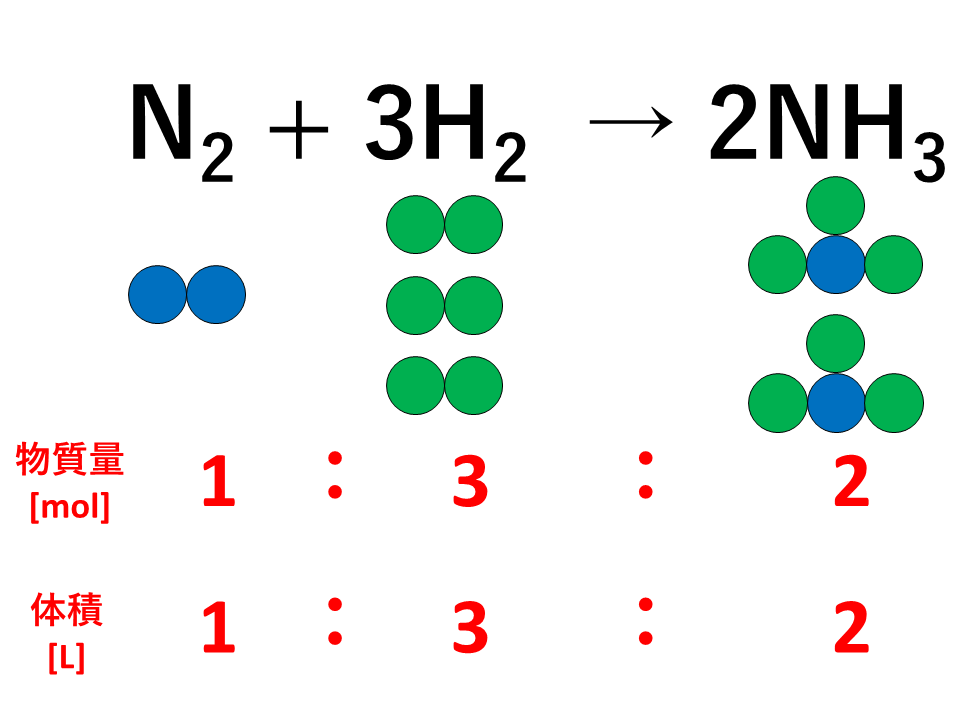
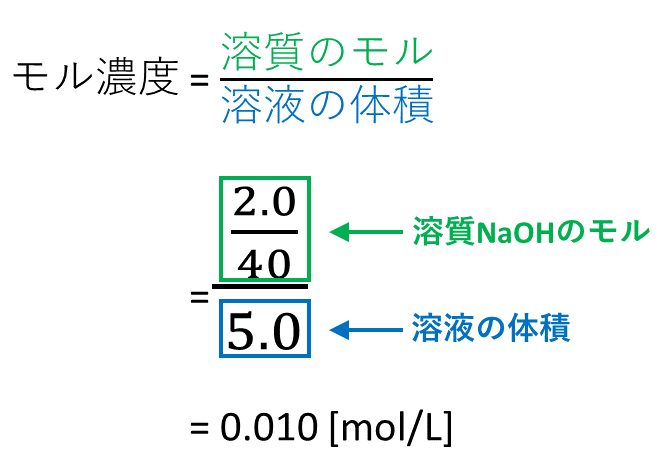
化学反応式の計算を考える際には、 必ず次の三つのことを考えてください 。 反応前の量mol 変化量mol 反応後の量mol mol と表記しましたが、反応式は元々分子の数についての式なので、 質量gなどではいけません 。 必ずmolで考えるようにし公式の覚え方教えてください mol濃度の公式も教えてください お願いします 回答 Hx 5年以上前 物質量 (mol)=質量 (g)÷原子量 (g/mol) 物質量 (mol)=質量 (g)÷分子量 (g/mol) 物質量 (mol)=体積 (L)÷224 (L/mol) モル濃度 (mol/L)=物質量 (mol)÷体積 (L) 単位に注目すると、理解しやすいと思います。 スラッシュ (/)は「割る÷」という意味なので、 モル濃度の単位はmol/L つまり mol÷L で求め 濃度のはなし~高校生向け モル濃度と質量モル濃度について~ 21年2月1日 学習内容解説ブログサービスリニューアル・受験情報サイト開設のお知らせ 学習内容解説ブログをご利用下さりありがとうございます。 開設以来、多くの皆様にご利用いただい
モル 公式 覚え方のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 |  |  |
 |  | |
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 | ||
 |  | |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 |  | |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
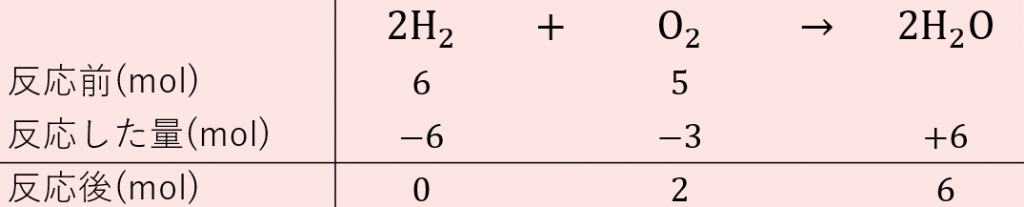 |  |  |
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 | ||
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  | |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 |  |  |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  | |
「モル 公式 覚え方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |
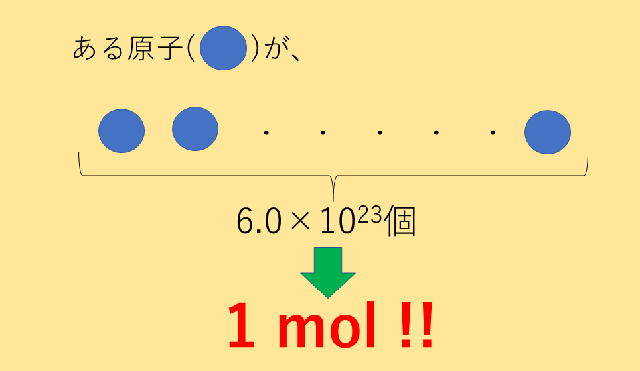
3年以上前 単位をよく見ることです。 mol/Lというのは分母にL、分子にmolという単位がある分数と考えられます 濃度mol/Lに体積Lを掛けたら、分子と分母が約分できるのでmol/L×L=molとなります。 今までやってきた単位換算はすべてこの関係にあります。 時間×速さ=距離とかも同じです。 Mana 3年以上前 ありがとうございます この回答にコメントする1モルとは 1mol(モル)とは、602×1023個の集団のことを表します。 物質量 mol(モル)を単位として表した物質の量のことを物質量(ぶっしつりょう)といいます。 記号は\(n\)を用います。 昔は物質量のことをモル数といっていました。 物質量の概念を鉛筆の数え方で例えてみましょう。 鉛筆は12本の集まりで1ダースと表現しますが、化学の世界では602×1023個の
Incoming Term: モル 公式 覚え方,




No comments:
Post a Comment